-
Články
Top novinky
Reklama- Vzdělávání
- Témata
Top novinky
Reklama- Volná místa
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaKlonovaná opice se poprvé dožila dospělosti. Budeme za chvíli schopni klonovat lidi?
4. 3. 2024
Makak pojmenovaný ReTro, který přišel na svět jako výsledek klonovacího experimentu čínských vědců, se dožil dospělosti. Jedná se o první takto úspěšné klonování, jež může být vstupní branou do dalšího výzkumu primátů. Co za úspěchem vědců stojí? A znamená to, že bychom byli schopní úspěšně klonovat lidi?
Nízká míra přežití klonů
Standardní klonovací technika, která byla použita například pro první savčí klonování ovce Dolly, využívá přenos jader somatických buněk (SCNT − somatic cell nuclear transfer). Zjednodušeně řečeno, izolované jádro dospělé somatické buňky (např. kožní, jaterní či tukové) se přenese do vajíčka, které předtím bylo zbaveno svého jádra, a toto vajíčko se implantuje náhradní matce. Postup však vede k extrémně nízkému počtu narozených a přeživších klonovaných embryí.
U primátů je úspěšnost obzvláště malá, jmenovitě u makaků rhesus do této doby neexistoval žádný životaschopný SCNT jedinec. V roce 2022 se sice podařilo dovést klon až k porodu, mládě však do 12 hodin uhynulo. Když vědci v roce 2018 klonovali makaky dlouhoocasé, vytvořili 109 klonovaných embryí a téměř tři čtvrtiny z nich implantovali do 21 náhradních matek, výsledkem bylo pouhých 6 těhotenství a pouze 2 z těchto opic přežily porod.
InzerceRozdíly v epigenetických modifikacích
Výzkumníci z Čínské akademie věd v Šanghaji se proto rozhodli porovnat 484 embryí makaka rodu rhesus, připravených technikou SCNT, s 499 embryi vzniklými standardní fertilizací in vitro, při které se spermie injikuje přímo do vajíčka (ICSI − intracytoplasmic sperm injection). Oba typy embryí před implantací náhradní matce prošly podobnými vývojovými stadii. Implantace však byla úspěšná pouze u 35 zárodků SCNT (oproti 74 embryím ICSI) a porodu se také dožilo méně plodů připravených technikou SCNT.
Vědci tedy provedli rozsáhlou genetickou analýzu SCNT embryí, která odhalila významné rozdíly v epigenetických modifikacích. To jsou změny, které upravují aktivitu genů, aniž by měnily strukturu DNA – např. methylace DNA nebo acetylace histonů. Právě methylace DNA byla u SCNT embryí snížená. Došlo také ke ztrátě imprintingu (za normálních okolností se některé geny pocházející od otce a od matky během vývoje exprimují odlišným způsobem), a to zejména v tkáni placenty. Kromě toho histologické vyšetření placent SCNT zárodků poukázalo na jejich nápadnou hyperplazii a kalcifikace.
Úprava placenty jako řešení
Vědci se proto rozhodli nahradit trofoblast (vnější vrstvu buněk časného embrya, ze které se později vyvine velká část placenty) SCNT embryí zdravým trofoblastem embryí připravených pomocí ICSI (viz obr.). U embryí SCNT se poté vyvinula určitá forma přirozené placenty, ale fetus byl stále klonovaným plodem.
Obr. Schéma znázorňující postup výměny trofoblastu mezi opičími blastocystami připravenými pomocí technik ICSI a SCNT
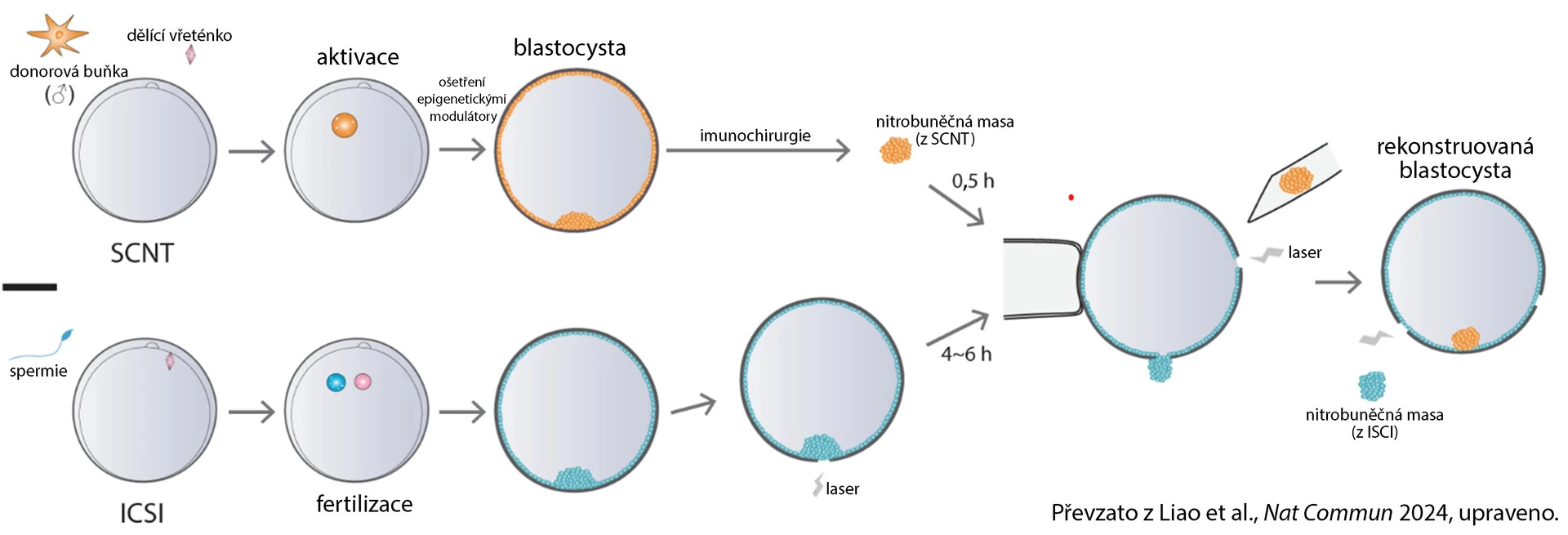
Tímto způsobem se podařilo připravit 113 embryí, z nichž 11 bylo implantováno 7 náhradním matkám. Výsledkem byla 2 těhotenství. Z jednoho z nich se narodil právě makak ReTro, který se zatím dožil více než 2 let. Druhá náhradní matka nosila dvojčata, která však uhynula 106. den těhotenství.
Podařilo se dokázat, že výměna trofoblastu snižovala defekty placenty a methylace DNA. Efektivita celého procesu je však ještě nižší než u standardní SCNT.
Proč vůbec makaky klonovat?
Od klonování prvního primáta s využitím metody SCNT před 6 lety byly tyto opičí modely použity ke studiu nemocí, jako jsou deprese a úzkost, a také k hodnocení účinnosti a bezpečnosti léků včetně antidepresiv. Toto úsilí je motivováno snahou využívat pro prokázání účinku léčiv co nejméně zvířat bez interference genetických vlivů. Proces tvorby klonů však stále zahrnuje příliš mnoho překážek. I přes nejnovější pokroky proto dosud nebyla vyřešena efektivita klonování.
A co lidé?
Jak uvedl dr. Lluís Montoliu ze španělského Národního centra pro biotechnologie, popsaný experiment ukázal, že klonovat primáty je sice možné, ale dosáhnout úspěchu je extrémně těžké, což klonování lidí prakticky vylučuje. Podobné postupy jako ten výše popsaný by navíc na území EU vůbec nemohly být provedeny. Evropská legislativa totiž vylučuje využívání primátů pro vědecké účely, pokud nejde o výzkum život ohrožujícího onemocnění lidí nebo primátů samotných.
Prof. Robin Lovell-Badge z britského Ústavu Francise Cricka k tomu dodává, že publikovaná metoda čínských vědců nás nikterak neposunula směrem k reprodukčnímu klonování lidí. „Bylo by to neetické čistě jen z bezpečnostních důvodů. A proč by vůbec někdo chtěl klonovat konkrétní osobu? Klon by se možná svým vzhledem podobal dárci somatických buněk (podobně jako jednovaječná dvojčata, která však od sebe obvykle snadno rozlišíme), ale neměl by stejný charakter, protože nejsme jen produktem svých genů.“
Autoři výzkumu navrhují prozkoumat potenciál výměny trofoblastu pro techniky asistované reprodukce v případech, kdy lidská embrya vykazují nedostatky ve vývoji trofoblastu.
(kata, este)
Zdroje:
1. Liao Z., Zhang J., Sun S. et al. Reprogramming mechanism dissection and trophoblast replacement application in monkey somatic cell nuclear transfer. Nat Commun 2024 Jan 16; 15 (1): 5, doi: 10.1038/s41467-023-43985-7.
2. Naddaf M. Nature Magazine. Meet ReTro, the first cloned rhesus monkey to reach adulthood. Scientific American, 2024 Jan 17. Dostupné na: www.scientificamerican.com/article/meet-retro-the-first-cloned-rhesus-monkey-to-reach-adulthood
3. Lovell-Badge R., Montoliu L. Expert reaction to study reporting that Chinese researchers have successfully cloned a rhesus monkey. Science Media Center, 2024 Jan 16. Dostupné na: www.sciencemediacentre.org/expert-reaction-to-study-reporting-that-chinese-researchers-have-successfully-cloned-a-rhesus-monkey
Líbil se Vám článek? Rádi byste se k němu vyjádřili? Napište nám − Vaše názory a postřehy nás zajímají. Zveřejňovat je nebudeme, ale rádi Vám na ně odpovíme.
Nejčtenější tento týden- Přehlížená pankreatitida koček: management péče v kostce − krok za krokem
- Management mykotických infekcí močových cest u psů a koček na základě aktuálních poznatků
- Nejčastější nádory očních víček u psů a koček
- Top 5 nejčastějších poranění svalů a šlach u psů
- Jak na kolaps trachey u psů?
Přihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání
