Molekulární analýza klonality lymfocytů
Odlišit reaktivní a neoplastickou proliferaci lymfocytů může být v některých případech obtížné. Jednou z možností je stanovení klonality lymfocytů. Tato metoda je založena na skutečnosti, že nádorová populace je monoklonální, čili vznikla expanzí jediné buňky, kdežto fyziologická, reaktivní populace lymfocytů je polyklonální.
Antigenové receptory lymfocytů a jejich variabilita
Antigenové receptory T a B lymfocytů jsou složeny z řetězců, jež jsou každý kódovaný lokusem v odlišné oblasti chromosomu. Na rozdíl od jiných genů nemají geny antigenových receptorů lymfocytů konstantní nukleotidové sekvence. Každý řetězec je vytvořen přeskupením několika menších genových segmentů, a tím se vytvoří jedinečná sekvence. Existují celkem 4 typy těchto genových segmentů: V (variable), D (diversity), J (joining) a C (constant). Během genové přestavby je náhodně vybráno z každé skupiny po jednom segmentu a ty jsou pak spojeny v pořadí V–D–J. Vzniká tak tzv. komplementaritu určující oblast 3 (CDR3), jež je unikátní pro každý klon lymfocytů a determinuje specificitu antigenového receptoru. Tato oblast je pak ještě spojena s konstantním segmentem C. Výsledkem složité kombinace jsou zcela unikátní sekvence DNA kódující obrovské množství antigen-specifických receptorů. Tento proces tak zajišťuje značnou biologickou variabilitu a umožňuje fungování adaptivní imunity.
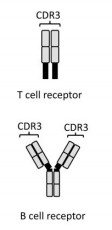
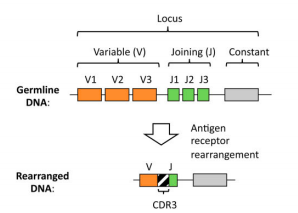
Molekulární analýza klonality
Molekulární analýza klonality vizualizuje rozmanitost antigenových receptorů. Analýza využívá amplifikace CDR3 polymerázovou řetězovou reakcí (PCR) a následnou elektroforetickou separaci fragmentů. Při reaktivní imunitní odpovědi jsou aktivovány klony mnoha různých lymfocytů, které se liší délkou CDR3; při PCR tak vznikají amplikony různých délek a tvoří tzv. polyklonální křivku. Naopak při nádorových procesech jsou lymfocyty odvozeny od jediné buňky, a mají tudíž identické CDR3. Při PCR se proto tvoří amplikony stejné velikosti, které generují tzv. klonální peak. Metoda PCR využívá dva primery definující oblasti (V a J), amplifikace pak proběhne jen v přestavěných úsecích. Základem je identifikace přeskupení segmentů V a J k výběru potřebných primerů. Pro optimální návrh analýzy a interpretace testů klonality je definování segmentů V a J zásadní.
Vzorky a provedení analýzy
Test klonality se provádí z genomové DNA. Jako vstupní materiál lze využít cytologické i histologické tkáně, biopsie nebo tělní tekutiny, které obsahují „podezřelé“ lymfocyty. DNA by měla být extrahována z částí vzorku, jež byly mikroskopicky vyšetřeny, aby bylo možné porovnat morfologické, imunofenotypizační a molekulární nálezy. Barvení ani zmražení vzorkům neškodí. Tkáně fixované formalinem a parafinem mají fragmentovanou DNA a nejsou pro analýzu ideální. Vhodné nejsou ani tkáně, které obsahují velké množství normálních lymfocytů (mízní uzliny). Teoreticky je nejvhodnější do testování klonality zahrnout všechny lokusy antigenových receptorů, jež kódují B a T lymfocyty. Nicméně ve veterinární medicíně je vyšetření výrazně limitováno financemi. Proto je zařazení imunofenotypizace před analýzou klonality nezbytné pro optimální výběr cíle a také pro správnou interpretaci výsledků klonality. U B lymfocytů se analýza zaměřuje na lokus IGH (těžký řetězec receptorů B lymfocytů), u T lymfocytů na lokus TRG.
PCR by měla probíhat minimálně v duplikátech, aby bylo možné odhalit tzv. pseudoklonalitu (amplifikace jen několika málo přeskupení, což může být chybně interpretováno jako klonální přeskupení).
Indikace a limitace metody
Testování klonality lymfocytů by nemělo být prvním ani jediným nástrojem v diagnostice lymfoidních malignit. Význam má při hodnocení netypických, smíšených nebo maturovaných lymfoproliferací, zejména v případech, kdy je obtížné je odlišit od reaktivní proliferace fyziologických lymfocytů. Testování klonality může být využito i pro sledování neoplastických klonů v čase (monitorování vývoje onemocnění a účinnosti terapie) nebo v různých anatomických lokacích. Výsledek testu je vždy nutné posuzovat s ohledem na klinický nález a morfologické i imunofenotypové charakteristiky vzorku.
(eza)
Zdroj: Keller S. M., Vernau W., Moore P. F. Clonality testing in veterinary medicine: a review with diagnostic guidelines. Vet Pathol 2016 Jul; 53 (4): 711−725, doi: 10.1177/0300985815626576.
Líbil se Vám článek? Rádi byste se k němu vyjádřili? Napište nám − Vaše názory a postřehy nás zajímají. Zveřejňovat je nebudeme, ale rádi Vám na ně odpovíme.
- Kožní atopický syndrom koček (FASS) − diagnostika a léčba environmentálně podmíněné formy
- Nejčastější nádory očních víček u psů a koček
- Top 5 nejčastějších poranění svalů a šlach u psů
- Top 5 situací využití gabapentinu ve veterinární praxi... a kdy naopak vhodný není
- Jak na kolaps trachey u psů?
